导读
脑动静脉畸形(BAVM)是一种具有生命威胁性的先天性脑血管疾病,其特征为动脉与静脉之间存在异常直接连接,导致出血、癫痫发作以及神经功能障碍等严重并发症。目前,BAVM的治疗主要依赖于血管内介入治疗和开颅显微手术,然而这些治疗手段具有侵入性,并且存在引发神经并发症的风险。近期研究揭示,大约80%的BAVM患者畸形血管团的内皮细胞中存在体细胞KRAS突变。这一发现突显了MEK抑制剂作为针对携带KRAS突变的BAVM患者治疗策略的潜在价值。然而,这些突变在BAVM组织中的等位基因频率相对较低(<10%),且在从血细胞中提取的DNA中难以检测。因此,目前BAVM的分子诊断仍然依赖于手术切除的组织样本。不幸的是,BAVM组织的手术切除可能面临诸多挑战,并伴随多种并发症,对于深部病变而言,并非总是可行的。因此,迫切需要开发一种非侵入性方法以准确识别遗传特征,实现早期靶向治疗。
北京天坛医院在《Nano Today》期刊上发表了题为“Utility of circulating plasma cell-free DNA for detection and quantification of brain arteriovenous malformations”的研究文章。该研究利用数字PCR技术,以外周血为样本,成功开发了一种用于检测和量化脑动静脉畸形的BAVM液体活检新方法。

研究亮点:
• 本研究采用数字PCR技术,验证了基于循环游离DNA(cfDNA)的脑动静脉畸形(BAVM)分子诊断方法的可行性,为突变评估提供了一种简便且侵入性较低的途径。
• 除了确认BAVM组织中已知的体细胞突变,本研究还揭示了基于数字PCR(dPCR)的分子诊断技术在术前一线诊断检测中的应用潜力,有助于明确组织变异的类型。
• 通过dPCR检测,确诊为KRAS突变的患者能够接受靶向治疗,有助于减少手术或介入治疗可能引发的高死亡率和致残风险。
方法及结果:
作者采用微滴数字PCR(dPCR)技术,评估了从31例患者的BAVM组织中提取的基因组DNA样本中KRAS p.G12D和p.G12V变异的存在情况。
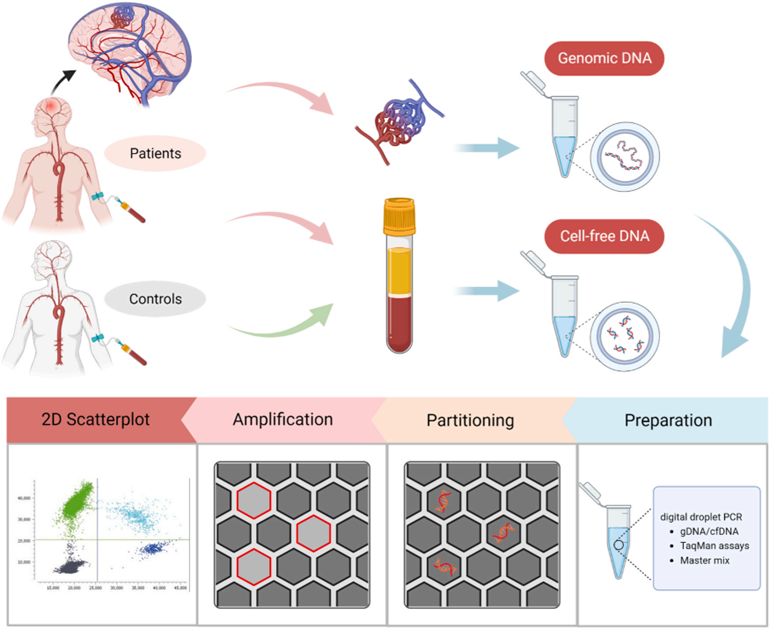
样本收集、处理及研究路径
研究结果显示,在对组织样本进行检测的过程中,31例脑动静脉畸形(BAVM)患者的组织样本中,有24例(占77%)被发现存在KRAS体细胞突变,这一发现与先前相关研究的结论相一致。在这些携带KRAS突变的患者中,15例(占63%)的循环游离DNA(cfDNA)在微滴式数字PCR检测中显示出至少2个与相应组织样本中突变类型一致的阳性微滴。相比之下,在对照组的50名受试者中,未发现任何样本的阳性微滴数量超过2个。
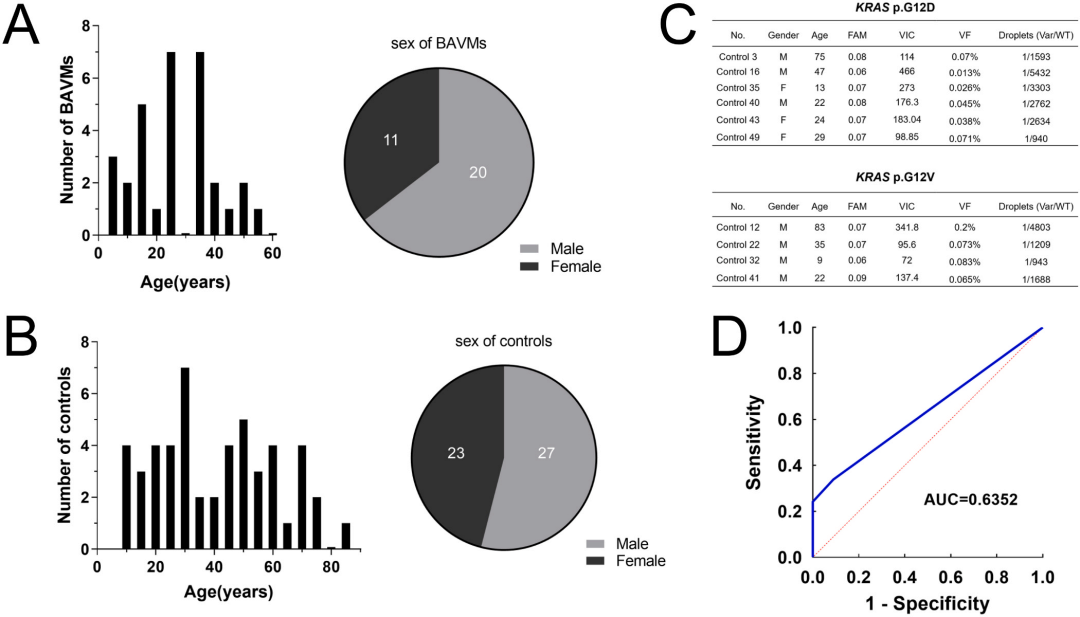
BAVM患者和对照组的人口和检测统计
采用数字PCR技术对脑动静脉畸形(BAVM)患者的循环游离DNA(cfDNA)进行检测,其检测灵敏度达到63%,特异性为100%,阳性预测值为100%,阴性预测值为81%。
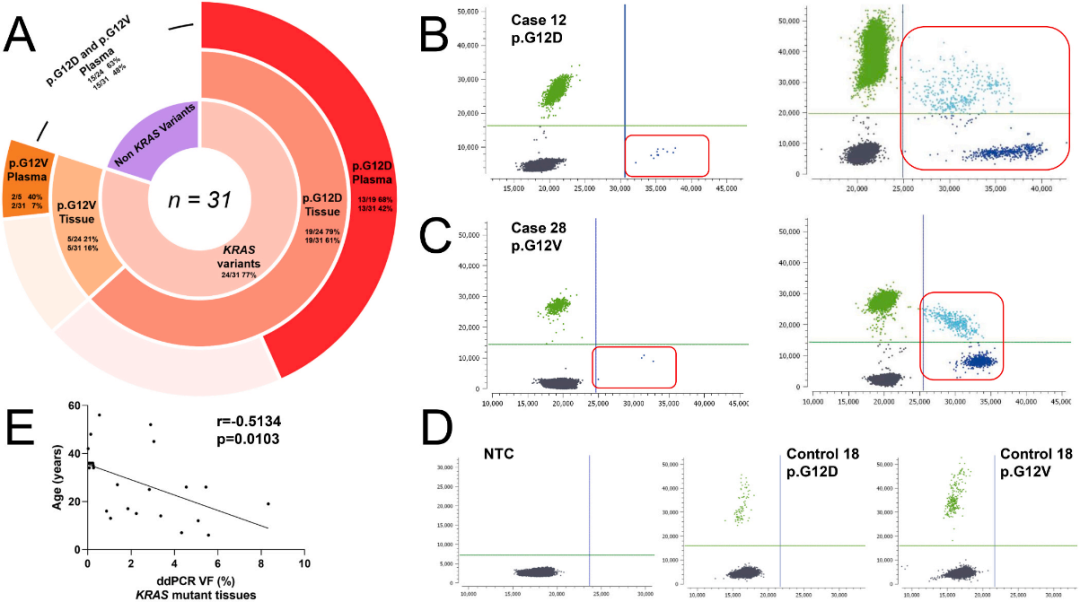
dPCR结果和数据统计
结论和展望:
本研究成功识别出源自脑动静脉畸形(BAVM)患者血浆循环游离DNA(cfDNA)中的致病性体细胞激活的KRAS变异。此外,基于数字PCR技术的BAVM液体活检诊断方法的应用,预期将推动个性化治疗方案的开发,并为阻止、减缓或延缓疾病进展的新策略提供潜在机会。